2023年9月15日,ACS Catalysis(一区TOP,IF=12.9)发表了9778818威尼斯杨志刚课题组最新研究成果,论文题目为“Switchable Nucleophilic Site Enables Expedient Synthesis of CF3‑Containing Thiazoles and Allenes from 1,3-Enynes”,该研究开发了一种由1,3-烯炔、亲电性CF3试剂和TMSNCS通过多组分反应来高效构建三氟甲基噻唑和联烯的新方法。并对其开展体内体外抗肿瘤活性评价,部分化合物能有效地抑制肿瘤生长,对肿瘤深层治疗具有巨大潜力。

在有机分子中适当地引入氟原子或含氟基团后,可以明显地影响分子的构象、降低pKa值、提高分子本身固有的能效和膜通透性;阻断易代谢位点从而改变药物代谢的途径及代谢速度,并通过分子间氢键的作用,延长药物在体内的保留时间,提高药物的生物利用度和选择性。然而,到目前为止从自然界中分离出来的含氟有机化合物只有12个,除此之外的所有含氟化合物都是需要人工合成得到,因此发展高效、绿色、经济的合成含氟分子的方法具有重要意义。
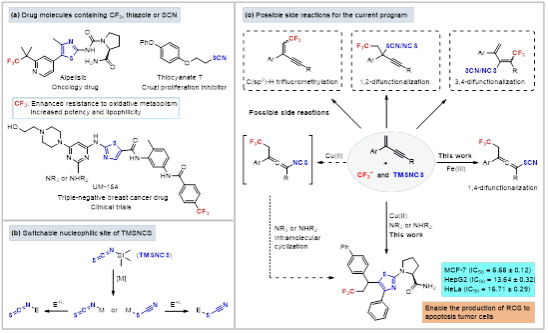
通常情况下,TMSNCS 被用作硫氰酸根负离子给体(─S─C≡N),它能与各种亲电试剂反应形成硫氰酸酯化合物。然而,它或许也能作为异硫氰酸根(-N=C=S)试剂源,这方面的工作目前报道相对较少。值得一提的是,异硫氰酸盐通常通过烯丙基或丙炔基硫氰酸酯的热异构化如:1,3-迁移转化得来。要是能对TMSNCS的亲核位点实现精确的控制,这将非常具挑战性,也具有非常好的工业应用前景。
基于这些科学问题,该课题组发展了一种金属催化剂精确调控TMSNCS亲核位点的方法,能够高效地实现1,3-烯炔、TMSNCS 和亲电的三氟甲基试剂的多组分反应,构建一系列三氟甲基化的噻唑和硫氰酸酯联烯。在廉价的铁(III)或铜(II)催化作用下,该反应既实用又方便,可与各种带有敏感官能团的底物兼容,也能对复杂的生物活性分子或天然产物进行后期修饰。
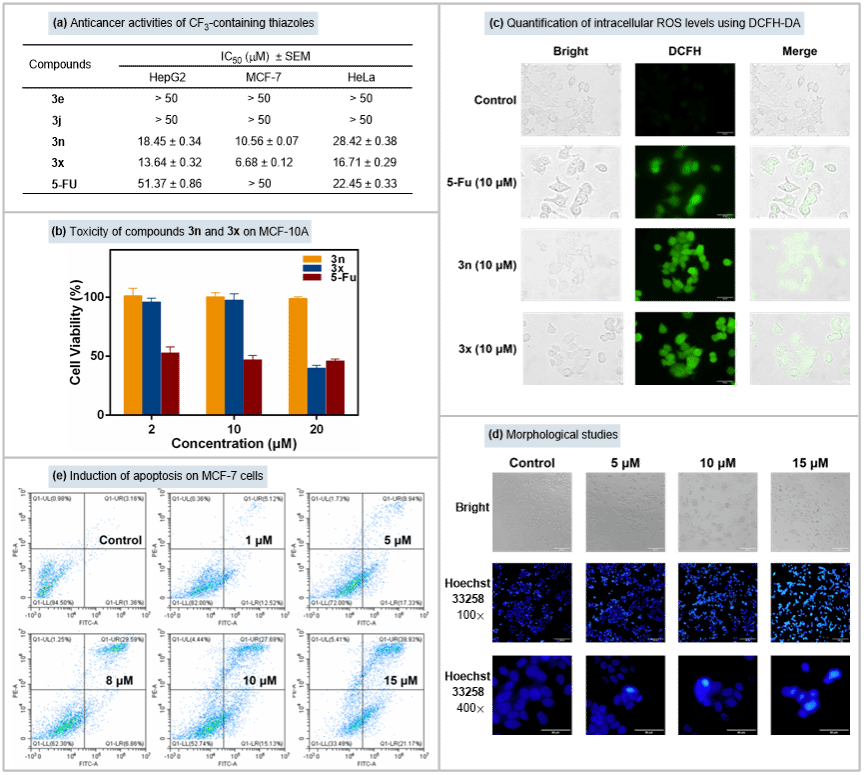
作者也对得到的含氟化合物进行生物活性评价,发现两个含CF3的噻唑化合物对三种人类癌细胞株具有显著的抑制活性,尤其对乳腺癌增殖具有较好的抑制作用,其效果超过了常见的含氟抗肿瘤试剂5-氟尿嘧啶(5-FU)。这两个化合物都提高了 MCF-7 细胞中活性氧(ROS)的水平,而这被认为是肿瘤细胞凋亡的早期步骤。这种新型的含CF3的噻唑类化合物可能会成为具有广泛应用前景的先导化合物,值得在未来的抗癌药物研发中进行进一步的结构调整和生物学研究。
9778818威尼斯2020级硕士生李翔宇、2021级硕士生李娜为该论文共同第一作者;9778818威尼斯杨志刚副教授为该论文通讯作者。周海兵教授、江中兴教授、邹有全教授、沈坤副研究员为本课题提供了指导和技术支持。
文章链接:https://pubs.acs.org/doi/10.1021/acscatal.3c03497